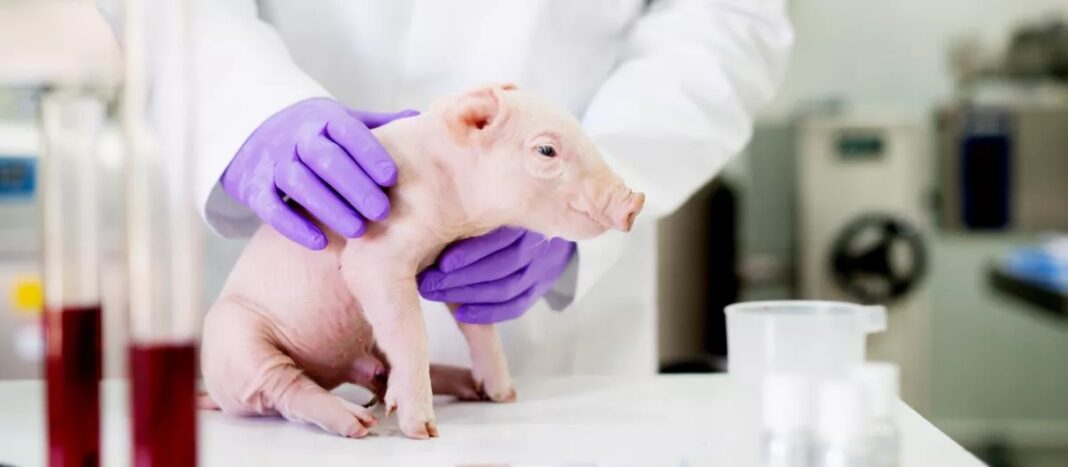
Un equipo del Reino Unido logró reemplazar de forma segura una sección completa del órgano y restaurar su función normal, incluida la deglución.
El procedimiento, realizado con éxito en ocho cerdos, consiste en la eliminación de las células del órgano de un donante, la repoblación con las propias células del receptor y su implantación posterior. Si esta tecnología se adapta para su uso en humanos, podría servir de ayuda en el tratamiento de recién nacidos o niños que nacen con atresia de esófago, una malformación congénita grave en la que el esófago no se desarrolla correctamente. Los resultados se publicaron en la revista científica Nature Biotechnology.
El logro se apoyó en una estrategia de ingeniería biológica que combinó tres pasos decisivos. El primero consistió en tomar esófagos de cerdos jóvenes y retirar todas las células originales mediante un proceso químico. De esa manera quedó solo la matriz extracelular, una estructura tridimensional que conserva la forma y la rigidez del órgano pero carece de componentes que podrían provocar rechazo. En paralelo, los investigadores obtuvieron pequeñas biopsias de músculo y tejido conectivo de los mismos animales que luego recibirían el implante. A partir de esas muestras generaron dos tipos de células madre capaces de transformarse en músculo, nervios y tejido estructural.
Esas células se inyectaron en el andamio porcino (la parte del esófago extraída a otros cerdos) siguiendo un patrón milimétrico, con cientos de microinyecciones distribuidas en toda la circunferencia y a lo largo del segmento. Con el tiempo fueron cubriendo la estructura y formaron un injerto celularizado. Luego, ese injerto pasó por un bioreactor diseñado para mantenerlo en rotación y con un flujo constante de nutrientes y oxígeno. Según describió Nature, durante esa etapa las células adquirieron un estado que favorece la formación de vasos sanguíneos, un paso indispensable para que el tejido sobreviva una vez implantado.
Cuando el injerto estuvo listo, los cirujanos retiraron 2,5 centímetros del esófago original de cada animal y colocaron en su lugar el segmento bioingenierizado. Para favorecer la vascularización lo envolvieron con una fina capa del propio tejido pleural del cerdo y colocaron un stent biodegradable dentro del esófago para mantener el conducto abierto durante las primeras semanas. Cinco de los ocho animales sobrevivieron al período completo de seguimiento, que duró seis meses, y pudieron tragar líquidos y alimentos sólidos, crecer al ritmo esperado y recuperar funciones que hasta ahora nadie había logrado reproducir con un órgano creado en laboratorio.
Los estudios posteriores mostraron que el injerto desarrolló músculos, nervios y vasos sanguíneos nuevos y que la estructura comenzó a parecerse cada vez más a la de un esófago natural. En las pruebas de manometría, que registran la presión interna durante la deglución, se observó una onda continua de contracción atravesando el segmento implantado.
Para los especialistas, esa señal demuestra que el injerto no solo resistía el paso de la comida sino que participaba activamente del movimiento que la impulsa hacia el estómago. Con el paso de los meses, “las propiedades biomecánicas del injerto se acercaron a las del tejido nativo”, indicaron los investigadores. Por su parte, el cirujano australiano Andrew Barbour, quien señaló que “la capacidad de generar un esófago con los componentes necesarios y con funcionamiento normal es notable” y que las zonas de cicatrización iniciales, que podían dificultar la deglución, “se redujeron con el tiempo”.
Aunque el estudio abre una vía concreta hacia futuros tratamientos, los investigadores reconocen que todavía deben resolver desafíos importantes. El propio Paolo De Coppi, uno de los investigadores al frente del estudio, dijo a Nature que el equipo trabaja para fabricar segmentos más largos, de entre 10 y 15 centímetros, como los que suelen necesitar los pacientes.
Ese objetivo exige desarrollar redes vasculares más extensas y sistemas de soporte adicionales. También falta comprobar cómo se comporta un injerto durante períodos más prolongados, algo indispensable para una futura aplicación clínica. El grupo prepara la transición hacia los primeros ensayos en personas, que, según indicaron, podrían comenzar dentro de tres o cuatro años si los resultados en animales se mantienen consistentes.